金属及其化合物计算17:
铬铁矿粉制备K2Cr2O7的产率计算之元素守恒
张新平
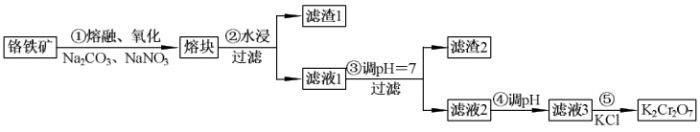
例题1:[2017•新课标Ⅲ.T27.节选]重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO•Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
回答下列问题:
(1)步骤①的主要反应为:
FeO•Cr2O3+Na2CO3+NaNO3;) Na2CrO4+Fe2O3+CO2+NaNO2。上述反应配平后FeO•Cr2O3与NaNO3的系数比为 。该步骤不能使用陶瓷容器,原因是 。
Na2CrO4+Fe2O3+CO2+NaNO2。上述反应配平后FeO•Cr2O3与NaNO3的系数比为 。该步骤不能使用陶瓷容器,原因是 。
(2)某工厂用m1 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品 m2 kg,产率为 ×100%。
【答案】(1)2:7 ;二氧化硅与碳酸钠高温下反应生成硅酸钠和二氧化碳。
(2)[m2/(m1×0.4×294g/mol÷152 g/mol)]。
解析如下:近年高考中经常出现产率等计算。



例题2:把6.62 g铁矿石样品投入适量的盐酸中,充分反应后过滤,再在滤液中加过量的NaOH溶液,充分反应后,过滤、洗涤、灼烧得4.80 g Fe2O3。现以该铁矿石为原料炼铁,若生产过程中铁元素损失4%,计算每生产1.00 t生铁(含铁96%),至少需要这种铁矿石多少吨?(结果保留两位小数)
解析如下:


金属及其化合物计算17:铬铁矿粉制备K2Cr2O7的产率计算之元素守恒.docx