作者其他文章
[转]电动汽车的希望:锂-空气电池
发布者:张新平发布时间:2017-11-06 19:56:28阅读(1249) 评论(1) 举报
电动汽车的希望:锂-空气电池
原创 2017-10-25 王晴,张馨文等 化学教育期刊
电动汽车的希望:锂-空气电池
王晴1,2 张馨文1,3 王明召1
1.北京师范大学化学学院 北京 100875
2. 海拉尔第二中学 内蒙古呼伦贝尔 021000
3.新东方集团 北京 100875
摘要
以高中化学电化学知识为基础,介绍一种学界预期将对电动汽车储能领域产生革命性影响的可逆电池——锂-空气电池的基础知识,涉及这种电池的基本结构、工作原理、电极反应、研究现状、发展前景等内容。
关键词
高中化学;电化学;锂-空气电池;工作原理;电极反应
当今,人们正在研究一种新型电池,称为锂-空气电池。它的能量密度(能量密度指单位质量电池储存的能量)是锂离子电池的10倍,理论上有潜力成为能量密度最高的化学电池。此外,它还具有环境友好、可逆等优点,因而显示出良好的应用前景。这种电池是Littauer和Tsai在1976年就提出的,但一直进展缓慢。1996年,Abraham等人成功地引入有机电解质(也称非水系电解质),才使这类电池的研究进入快速发展时期[1]。2006年,Bruce等人采用有机电解质体系的锂-空气电池,验证了这类电池反应的可逆性,实现了50 次循环,比容量为600 mAh/g[2]。自此这类电池获得了广泛关注,学界评价它有望成为电动汽车的实用储能设备[3]。
1什么是锂-空气电池

图1 锂-空气电池模型
锂-空气电池是一种化学电池,通过锂和氧气之间的化学反应,将化学能转化成电能。它的基本结构如图1所示[4]。单质锂既是负极材料,又是负极反应物。正极材料为反应提供“场所”,常采用多孔碳材料。氧气是正极反应物,通常来源于空气,因此正极又称为空气电极,并且这种电池常称为空气电池。两极间的电解质常用锂盐的有机溶液。
选择锂作为负极的优势在于锂是质量最轻的碱金属,具有较高的比能量(单位质量所释放的能量),在提供相同电量时消耗的质量小,所以可望制成较轻的电池。而锂的性质活泼,放电时,失去电子的负极反应极易发生:Li - e- = Li+。
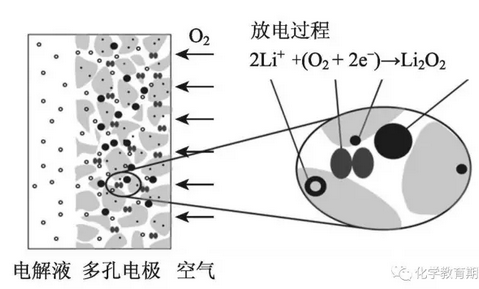
图2 多孔电极结构示意图
用作正极电极材料的多孔碳材料具有排列规则、大小可调的孔道结构[4],其结构示于图2。在放电时,氧气进入多孔电极的孔道内,在多孔电极表面获得外电路传来的、由金属锂在负极失去的电子,生成O2-。O2-再发生一系列反应,最终与电解质中的Li+结合,主要生成电极产物Li2O2。由于电极产物Li2O2在非水电解质中溶解性很差,会堵塞在电极的孔道内,阻止放电过程继续进行,因此这种多孔材料的孔径对电极过程能否持续发生至关重要。对于单位质量的正极材料,孔径小,拥有的孔就多,总的孔腔内表面积就大,为电极过程提供的反应活性位点就多,并且为催化剂提供的分散空间也大,因此有利于电极过程的进行。而孔径大则有利于气体顺畅流通,同时为生成的难溶性产物提供储存场所,以保证反应能持续的进行[5]。显然,高效电池需要正极材料具有适宜的孔径,正极多孔碳材料已经成为一个研究方向。
在非水电解质中,放电时,氧气在正极是如何被还原的?这个过程比较复杂,有些问题还在探索之中。目前普遍认可的是,放电时,氧气在正极表面获得电子,被还
原成超氧根离子O2-,O2-与Li+结合为超氧化锂LiO2:
O2+ Li+ + e—= LiO2
超氧化锂在溶液中不稳定,会转化成过氧化锂Li2O2,这可以通过以下2个过程实现[6]:
化学过程:2LiO2 = Li2O2+ O2
电化学过程:LiO2 + Li+ + e— = Li2O2
因此,放电时电池的总反应为:
2Li + O2 = Li2O2
近年来发现,放电产物Li2O2还可以继续获得电子,转化成氧化锂:
Li2O2+ 2Li+ + 2e- = 2Li2O
这样,电池反应就是:
4Li + O2 = 2Li2O
作为可逆电池,施加一定大小的外电压,就可以给这种电池充电。此时,电池的负极上发生放电反应的逆过程:Li+ + e- = Li。
电池的正极上发生的是生成氧气的反应,较稳定的放电产物Li2O2中的O22-失去电子,被氧化为氧气,Li+释放出来,电极反应为[2]:
Li2O2= 2Li+ + O2 + 2e-
这个正极反应所需能量较高,需要在较高的充电电压下才能发生,显然它决定了锂-空气电池的可逆性能否真正实现。事实上,正极需要使用合适的催化剂,来降低充电电压。如何更好地实现锂-空气电池的循环性,一直是一个研究重点[7]。
2研究取得了什么进展
近年,有关锂-空气电池的研究取得了令人振奋的进步,在此举一个研究实例[8]。2012年,英国圣安德鲁大学Bruce研究小组设计了一款锂-空气电池,以二甲基亚砜(DMSO)作电解液的溶剂,电解质溶质为高氯酸锂(LiClO4)或六氟合磷酸锂(LiPF6),以纳米多孔金作正极材料,金属锂作为负极,氧气的压强为101 kPa。该电池表现出良好的循环性能,需要的充电电压低,充电速率比以碳材料作电极的电池快。循环100次之后,仍拥有95%的容量。循环至第100次时,正极处生成的Li2O2纯度仍大于99%,且它在充电时可被完全氧化为氧气。该电池体系表现出如此优异的电化学性能,是得益于使用了纳米金电极和稳定性良好的电解液[1]。
这个电池使用纳米多孔金作正极材料。纳米多孔金是利用金属的活泼性差异而制得的。将金箔合金中的活泼金属溶解掉,在金纳米骨架里就留下了孔洞通道[9]。这种多孔金保留了金的可焊性、导电性、延展性、高结构强度、耐高温、高化学惰性等特点。作为电极,它具备电阻小、充放电过程中稳定、表面积大的多孔结构能为电极反应提供充足的场所、氧气及电解质可在空隙中顺利扩散等优点。相比于传统的多孔碳电极,纳米金做正极时,电极反应物Li2O2在充、放电过程中的形成和分解速度明显加快,使电池表现出了更好的循环性[8]。
电解液以有机物DMSO作为溶剂,其分子式为(CH3)2SO,结构式如图3所示。DMSO分子中的氧原子具有孤对电子,有较高的负电荷密度,容易与阳离子Li+发生相互作用,使锂盐易溶于其中。不含水的DMSO在80 ℃以下不会与负极金属锂发生副反应;挥发性低,损耗低;在充、放电过程中自身不会大量发生氧化还原反应,不会产生过多副产物而影响电池的充、放电效率。目前,对于金作为正极材料的锂-空气电池,DMSO已经成为最有潜力的电解质溶剂[11]。

图3 DMSO
前面已述,人们早就推测,放电时氧气在正极表面得电子时,首先生成的是超氧离子O2-,它与电解质中的Li+结合生成LiO2。O2-容易结合1个电子,转变为过氧离子O22-。Li+的正电荷密度大,它倾向于与负电荷密度大的阴离子成键。与超氧离子O2-相比,过氧离子O22-带的负电量更高,电荷密度更大。结果,LiO2迅速转变成更稳定的Li2O2。但是O2-非常活泼,存在时间短,通过常规方法很难检测到它[10]。放电时,氧气在还原过程中存在LiO2中间产物这个推论,一直没有得到实验证实,争论了40年[11]。
当采用LiPF6的DMSO溶液作为电解液时,Abraham等人首次捕获到了正极反应过程中的中间体超氧根离子O2-,结束了这场争论。他们提出,溶剂分子DMSO可通过氧原子与Li+配位,形成溶剂化大阳离子[Li(DMSO)n]+(n通常为4)。这种溶剂化离子的正电荷密度比Li+的低,因此该大阳离子可与负电荷密度较低的O2-形成较稳定的离子对[Li(DMSO)n +- O2-],延长了O2-的存在时间,从而可被仪器检测出来[6]。
3市场上有锂-空气电池商品了吗
目前,尽管锂-空气电池研究已经取得了令人振奋的进展,但是仍处于实验室研究阶段。学界预测,它成为便携式电池商品约需要10~15年,而满足电动汽车的供能要求,则可能需要超过35年[12]。走向实际应用面临很多挑战,待解决的问题包括:金属锂作为负极材料存在锂会形成非均相的枝状形态这一主要问题,这将导致危险的短路,并影响电池的循环性;金属锂活泼性高,在湿润的空气中不稳定;电极产物阻塞空气电极孔道,会导致充、放电过程提前终止;电极、电解质在充、放电过程中会发生分解;充电过程所需电压高,放电过程效率低等[13]。
人们正在努力寻找解决这些问题的方法,在此举一个成功的研究实例。2010年,Zhou[1]等人设计出了有机-水双电解质体系锂-空气电池。这种电池的负极金属锂处于有机电解质中,其溶剂是有机物碳酸乙烯酯/碳酸二甲酯(EC/DC),溶质是高氯酸锂(LiClO4)。该电池有2个新颖之处:(1)正极一侧使用KOH水溶液作为电解液,电极反应产物最终形成可溶的LiOH,解决了有机体系中正极反应产物不溶于电解液而阻塞电极微孔,导致放电过程提前结束的问题;(2)使用锂超离子导电玻璃薄膜来隔开两极。这种薄膜只允许Li+通过,阻止空气中的H2O、O2通过,避免了它们与金属锂电极发生反应。
2014年,该研究组使用新材料掺氮石墨烯纳米片(N-GNSs)作为该体系电池的正极电极材料[15]。石墨烯是一种单碳原子厚度的片层材料,层内结构与石墨中的单层相同,每个碳原子与相邻的3 个碳原子成键,组成平面六边形共轭结构。石墨烯片层的厚度一般为0.35 nm左右,是目前最薄的二维材料。电子穿过这样薄的石墨烯时,几乎不存在任何阻力,因此石墨烯导电时产生热量少,导电效率高,是已知导电性能最优异的材料。将N引入石墨烯,让氮原子取代六边形网格结构中的部分碳原子,就得到掺氮石墨烯。由于N与C的原子大小以及价态的区别,N的引入使石墨烯的结构发生了一些改变,所以掺氮石墨烯表现出更好的导电性和稳定性。此外,掺氮石墨烯对O2的还原反应还具有催化作用。在石墨片层中,有些部位的碳原子缺失,本应与缺失碳原子相连的碳原子变得成键不饱和,晶体偏离理想周期结构,这称为缺陷。这种成键不饱和的碳原子容易与氧原子结合生成含氧基团(C—O,C=O和O=C—O),而N的引入使得不饱和碳原子增多,因此使O2更易于被还原。同时,N的电负性比C强,氮原子在网格结构中会将成键电子吸引过来,使与它成键的碳原子带上一定的正电荷。此类碳原子对带有孤对电子的氧气分子具有吸引力,可通过与孤对电子结合而将O2吸附住。这种吸附作用削弱了O2内部的O=O键,使O2活化,也使O2的分解反应变得更容易。目前,掺氮石墨烯已成为锂-空气电池领域广泛研究的正极电极材料[16]。
经实验,该电池不间断放电30 min后,仍能维持输出电压高于2.2 V,表现出较好的可循环性。
尽管目前还存在这些问题,学界认为,锂-空气电池一旦研发成功并实现商业化,它将对电能存储领域产生革命性的影响[17]。
参考文献
[1] 杨凤玉,刘清朝,徐吉静,等.科学通报,2013,58(31):3199-3212
[2] Ogasawara T,Débart A,Holzapfel M,et al.J.Am.Chem.Soc.,2006,128(4):1390-1393
[3] Bhatt M D,Geaney H,Nolan M,etal.Phys.Chem.Chem.Phys.,2014,16(24):12093-12130
[4] GirishkumarG,Mc Closkey B,Luntz A C,et al.J.Phys.Chem.Lett.,2010,1(14):2193-2203
[5] Beattie S D,ManolesuD M,Blair S.J.Electrochem.Soc.,2009,156(1):A44-A47
[6] Laoire C O,MukerjeeS,Abraham K M,et al.J.Phys.Chem.C.,2010,114(19):178-186
[7] Black R,Lee J H,Adams B,etal.Angew.Chem.Int.Ed.,2013,120:410-414
[8] Peng Z,FreunbergerS A,Chen Y,et al.Sci.,2012,337(6094):563-566
[9] Ding Y,Kim Y J,Erlebacher J.Adv.Mater.,2004,16(21):1897-1900
[10] Trahan M J,MukerjeeS,Plichta E J,et al.J.Electrochem.Soc.,2013,160(2): A259-A267
[11] Peng Z,FreunbergeS A,Hardwick L J,et al.Angew.Chem.,2011,123(28):6475-6479
[12] Capsoni D,Bini M,Ferrari S,etal.J.Power Sources,2012,220:253-263
[13] Md A R,XiaojianW,Cuie W.J.Appl.Electrochem.,2014,44(1):5-12
[14] Wang Y G,Zhou HS.J.Power Sources,2010,195(1):358-361
[15] Eunjoo Y,HaoshenZ.RSC Adv.,2014,4:13119-13122
[16] 陈旭,何大平,木土春.化学进展,2013,25(8):1292-1301
[17] 郭丽敏,彭章泉.分析化学,2013(2):307-314
| 引用本文: |
| 王晴, 张馨文, 王明召. 电动汽车的希望:锂空气电池[J]. 化学教育(中英文), 2017, 38(17): 1-4 |
 鄂公网安备 42018502004132号
鄂公网安备 42018502004132号