教学随笔:
类比命题中有陷阱啊
张 新 平
某模拟题及解析如下:下列实验事实不能用平衡移动原理解释的是( )
A.向pH=4的乙酸溶液稀释10倍后溶液pH<5
B.相比较于常温,加热后的纯碱溶液去除厨房的油污的效果更好
C.对CO(g)+NO2(g)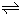 CO2(g)+NO(g)平衡体系压缩容器后可使气体颜色变深
CO2(g)+NO(g)平衡体系压缩容器后可使气体颜色变深
D.水垢中含有CaSO4,可先用Na2CO3溶液浸泡处理,而后用盐酸去除
【答案】C
【详解】A.将pH=4的乙酸溶液稀释10倍后,乙酸溶液的浓度减小,电离平衡正向移动,H+的物质的量增大,溶液pH<5,A不符合题意;
B.纯碱的主要成分为碳酸钠,溶于水发生水解CO32-+H2O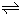 HCO3-+OH-,水解过程吸热,加热,水解平衡正向移动,c(OH-)增大,则热的纯碱溶液去污效果更好,B不符合题意;
HCO3-+OH-,水解过程吸热,加热,水解平衡正向移动,c(OH-)增大,则热的纯碱溶液去污效果更好,B不符合题意;
C.对于CO(g)+NO2(g)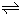 CO2(g)+NO(g),反应前后气体分子数相等,达平衡后加压,平衡不发生移动,但气体的浓度增大,所以气体颜色变深,C符合题意;
CO2(g)+NO(g),反应前后气体分子数相等,达平衡后加压,平衡不发生移动,但气体的浓度增大,所以气体颜色变深,C符合题意;
D.水垢中含有CaSO4,先用Na2CO3溶液浸泡处理,可发生转化CaSO4(s)+CO32-(aq)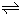 CaCO3(s)+SO42-(aq),增大c(CO32-),可将大部分CaSO4转化为CaCO3,而后用盐酸去除,D不符合题意;
CaCO3(s)+SO42-(aq),增大c(CO32-),可将大部分CaSO4转化为CaCO3,而后用盐酸去除,D不符合题意;
故选C。
点评:
看看这道题是如何掉进违背基本科学性的陷阱中的。
选项C源于H2(g)+I2(g)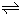 2HI(g)类比改编而来。
2HI(g)类比改编而来。
但命题者确忽视了2NO2(g)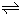 N2O4(g)这样一个科学事实。因此也就不能说明“对CO(g)+NO2(g)
N2O4(g)这样一个科学事实。因此也就不能说明“对CO(g)+NO2(g)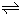 CO2(g)+NO(g)平衡体系压缩容器后可使气体颜色变深”中,没有平衡移动了。
CO2(g)+NO(g)平衡体系压缩容器后可使气体颜色变深”中,没有平衡移动了。