教学随笔:
如何理解化学规律中的一般性与特殊性
张 新 平

规律的一般性与特殊性共存,是人类社会发生发展的普遍性规律,也是自然规律。化学作为自然科学的一个门类,当然也不例外,化学规律中既有共性(一般性的规律)的,又有个性(特殊性的)的。也正因为如此,任何种群的延续需要“一般性”保持种群应有的属性,但是要想在物竞天择、优胜劣汰的自然界生生不息,又要有“与时俱进”变化与特性进化,才能保持种群立于不败之地。也正因为如此,才使得人类社会以及自然界的进化既保持相似的演变,同时又有五彩缤纷的神奇变异,呈现出多姿多彩的世界。
如地球的存在,就是普遍性(一般性)与特殊性共存的最好例证:

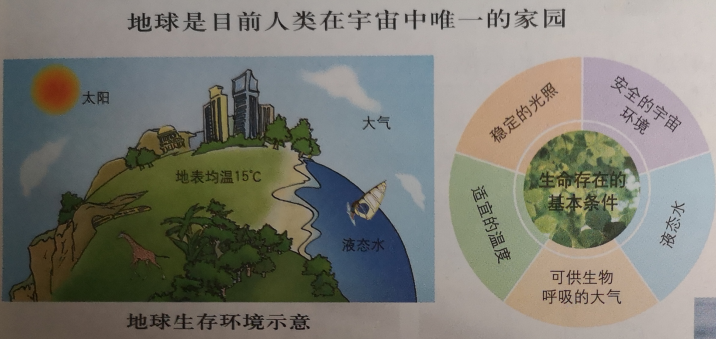
——周瑞祥 高俊昌.普通高中教科书·地理图册·必修第一册·北京:星球地图出版社,2019年第2版.P7。
如何理解化学规律中的一般性与特殊性呢?即既要注重学习过程中的相似性(一般性的规律)类比推理,又要明辨不同独立个体特殊性所决定的差异性。
高一学生在刚刚开始高中化学学习时,如学到铝与氢氧化钠溶液的反应方程式:
2Al+2NaOH+2H2O==2NaAlO2+3H2↑。
有命题为:已知铍(Be)的化学性质与铝相似,请写出铍与氢氧化钠溶液反应的化学方程式。
有很多同学的答案为:2Be+2NaOH+2H2O==2NaBeO2+3H2↑。
显然,在相似性类比的前提下,特殊性(个体个性)的明辨是类比结果正确的保证。
如1,一般原子都趋向于达到最外层8电子稀有气体型稳定结构,但不会因为有稀有气体He、以及H、Li、Be、B、金属Pd等的特殊性而被否定。
如2,盐酸是电解质的问题。
盐酸是电解质,“约定俗成”盐酸是电解质。
“给概念“下定义”与化学命名原则所遵循的道理是一致的,都应当从反应物质的本质属性并兼顾学术界公认的原则出发,而不应简单地从某一侧面、从形式逻辑的推论出发。……对待这类已有明文规定的问题,再另行立论,运用推理法来否定大家公认的科学结论是不可取的。”
纵观中学化学教材,对于盐酸是不是电解质,均避而不谈。是故意规避,还是另有隐情,不得而知。这也是导致一些执教者在教学、命题等中执着于“从形式逻辑的推论出发”,否定盐酸是电解质的原因吧!
——1983年第3期《化学教育》.“应当怎样认识“盐酸是电解质”这一结论?”P56.
关于离子反应:有人认为Na+H2O→无离子参加,否定离子反应的定义,要更改定义。该文发在《化学教育》,待查。
如3,酸性氧化物一般不与酸发生非氧化还原反应,但是有氢氟酸腐蚀玻璃:SiO2+4HF==SiF4↑+2H2O.
如4,一般多元弱酸(过量)与少量碱反应时生成的是酸式盐。如:
SO2+NH3·H2O==NH4HSO3 、CO2+NH3·H2O==NH4HCO3
CO2+NaOH==NaHCO3
因为如:CO2+2NaOH==Na2CO3+H2O,CO2+Na2CO3+H2O==2NaHCO3.
特殊:SiO2+2NaOH==Na2SiO3+H2O.不论碱多少,只能生成正盐。且强碱多盛放在玻璃瓶中,只是不能用磨口玻璃塞。光滑的玻璃瓶内壁应该是很难与强碱反应的,或者更准确的说是反应很慢很慢很慢!短时间内观察不到反应的结果。
如5,一般多元弱酸的酸酐加入(或通入)盐溶液中,首先生成正盐,过量后又转化为酸式盐。如:CO2(少)+2NaAlO2+3H2O==Na2CO3+2Al(OH)3↓,CO2+Na2CO3+H2O==2NaHCO3.
因此,通CO2过量时有总反应:CO2(过)+NaAlO2+2H2O==NaHCO3+Al(OH)3↓.
特殊性:CO2通入苯酚钠溶液中只能生成酸式碳酸盐。当然这是由于苯酚的酸性强于HCO3-的酸性而决定的。
如6,一般酸式碳酸盐的溶解度大于其正盐。但是Na2CO3的溶解度确大于NaHCO3,侯德榜制碱法就是利用了NaHCO3的溶解度较小易从饱和溶液中结晶析出来制碱的。
……